Quanto č utile/interessante questa discussione:
| Autore |
Discussione |
|
|
mredbull
Nuovo Arrivato

2 Messaggi |
 Inserito il - 29 giugno 2010 : 23:32:22 Inserito il - 29 giugno 2010 : 23:32:22




|
Ciao a tutti!
Ho una grossa difficoltŕ nello svolgere un esercizio di chimica organica sulla risononza, probabilmente per errori nella trascrizione degli appunti del professore, e il libro di testo non mi schiarisce il dilemma...Azz
Praticamente a lezione ho scritto che le configurazioni neutre piů stabili sono quelle con separazione di carica...
Quindi tra:
CH2=CH-O-CH3 ==>**CH2-CH=O*-CH3 (**C ha carica negativa; * O ha carica positiva), la piů stabile č quest'ultima.
Ma č vera questa cosa?
Hai fini della stabilitŕ relativa delle strutture limite di risonanza ho scritto che le
strutture piů stabili sono.
a)quelle che raggiungolo l'ottetto completo
b) strutture con minore separazione di carica
Io il punto B) proprio non lo lo capisco... non č che mi riuscite a dare una dritta?
Per esempio ho un esercizio con un fenolo, non ho nessun problema a fare le diverse strutture di risonanza, ma non riesco assolutamente a indicare la scala di stabilitŕ tra le diverse strutture...
|
|
|
|
|
nashita
Utente
 

Prov.: Puglia

1085 Messaggi |
 Inserito il - 30 giugno 2010 : 11:42:11 Inserito il - 30 giugno 2010 : 11:42:11




|
Citazione:
Messaggio inserito da mredbull
Ciao a tutti!
Ho una grossa difficoltŕ nello svolgere un esercizio di chimica organica sulla risononza, probabilmente per errori nella trascrizione degli appunti del professore, e il libro di testo non mi schiarisce il dilemma...Azz
Praticamente a lezione ho scritto che le configurazioni neutre piů stabili sono quelle con separazione di carica...
Quindi tra:
CH2=CH-O-CH3 ==>**CH2-CH=O*-CH3 (**C ha carica negativa; * O ha carica positiva), la piů stabile č quest'ultima.
Ma č vera questa cosa?
Hai fini della stabilitŕ relativa delle strutture limite di risonanza ho scritto che le
strutture piů stabili sono.
a)quelle che raggiungolo l'ottetto completo
b) strutture con minore separazione di carica
Io il punto B) proprio non lo lo capisco... non č che mi riuscite a dare una dritta?
Per esempio ho un esercizio con un fenolo, non ho nessun problema a fare le diverse strutture di risonanza, ma non riesco assolutamente a indicare la scala di stabilitŕ tra le diverse strutture...
Ciao, scusami ma come fa ad essere una struttura neutra a separazione di carica ? 
Tra le due strutture :
CH2=CH-O-CH3 ==>**CH2-CH=O*-CH3 (**C ha carica negativa; * O ha carica positiva)
la piů stabile č la prima ... l'ultima č instabile per due motivi :
1) č a separazione di carica
2)il suo atomo piů elettronegativo (O) č carico positivamente ...
Tant'č vero che l'ibrido di risonanza assomiglierŕ proprio alla prima struttura, piuttosto che alla seconda.
Del punto B cos'č che non ti č chiaro ?
Le strutture a separazione di carica, sono quelle meno stabili perchč possiedono un'energia piů alta per tenere separate le cariche opposte ...e una maggiore energia , corrisponde a una minore stabilitŕ.
Quindi quando ti trovi due strutture, di cui una carica e l'altra neutra , considerando il punto B da te enunciato, quella piů stabile č la neutra .
Se invece ti trovi una struttura neutra e due strutture a separazione di carica, avrai che la piů stabile č la neutra, poi quella a separazione di carica in cui le due cariche ( positiva e negativa) siano vicine, e poi per ultimo quella in cui le due cariche ( positive e negativ) siano lontane.
|
 |
 |
|
|
0barra1
Utente Senior
   

Cittŕ: Paris, VIIčme arrondissement

3847 Messaggi |
 Inserito il - 30 giugno 2010 : 12:56:35 Inserito il - 30 giugno 2010 : 12:56:35




|
Citazione:
Messaggio inserito da nashita
Quindi quando ti trovi due strutture, di cui una carica e l'altra neutra , considerando il punto B da te enunciato, quella piů stabile č la neutra .
Tant'č che prende il nome di Principio di Elettroneutralitŕ, formulato da Linus Pauling.
Citazione:
Messaggio inserito da nashita
Se invece ti trovi una struttura neutra e due strutture a separazione di carica, avrai che la piů stabile č la neutra, poi quella a separazione di carica in cui le due cariche ( positiva e negativa) siano vicine, e poi per ultimo quella in cui le due cariche ( positive e negativ) siano lontane.
Aggiungerei che tra le strutture a separazione di carica quella piů stabile č anche quella in cui la carica negativa č posizionata sull'atomo piů elettronegativo tra i due che effettivamente portano le cariche. |
 |
|
|
nashita
Utente
 

Prov.: Puglia

1085 Messaggi |
 Inserito il - 30 giugno 2010 : 13:04:22 Inserito il - 30 giugno 2010 : 13:04:22




|
Citazione:
Messaggio inserito da 0barra1
Citazione:
Messaggio inserito da nashita
Quindi quando ti trovi due strutture, di cui una carica e l'altra neutra , considerando il punto B da te enunciato, quella piů stabile č la neutra .
Tant'č che prende il nome di Principio di Elettroneutralitŕ, formulato da Linus Pauling.
Citazione:
Messaggio inserito da nashita
Se invece ti trovi una struttura neutra e due strutture a separazione di carica, avrai che la piů stabile č la neutra, poi quella a separazione di carica in cui le due cariche ( positiva e negativa) siano vicine, e poi per ultimo quella in cui le due cariche ( positive e negativ) siano lontane.
Aggiungerei che tra le strutture a separazione di carica quella piů stabile č anche quella in cui la carica negativa č posizionata sull'atomo piů elettronegativo tra i due che effettivamente portano le cariche.
questo č il terzo criterio ( i criteri vanno in ordine di prioritŕ), ovvero a paritŕ di separazione di carica, quella piů contribuente č quella con la carica negativa sull'atomo piů elettronegativo  |
 |
 |
|
|
mredbull
Nuovo Arrivato

2 Messaggi |
 Inserito il - 30 giugno 2010 : 13:48:26 Inserito il - 30 giugno 2010 : 13:48:26




|
Grazie per le risposte, mi avere chiarito il concetto!
Quindi in questo esercizio, dove devo stabilire l'ordine di prioritŕ,
Immagine:
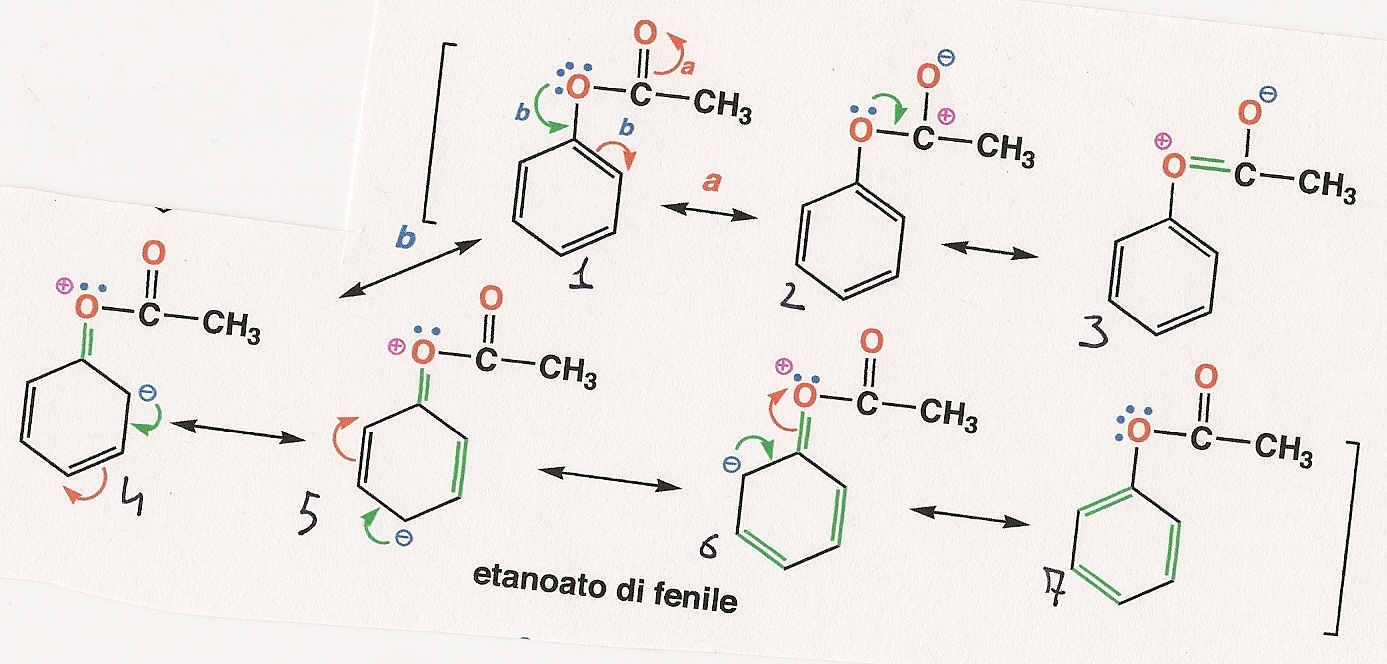
476,65 KB
avrň che le piů stabili sono la 1 la 2 e la 7
Con la 1 e la 7 piu stabili giusto? |
 |
|
|
nashita
Utente
 

Prov.: Puglia

1085 Messaggi |
 Inserito il - 01 luglio 2010 : 11:22:25 Inserito il - 01 luglio 2010 : 11:22:25




|
| giusto :D |
 |
 |
|
| |
Discussione |
|
|
|
Quanto č utile/interessante questa discussione:
| MolecularLab.it |
© 2003-18 MolecularLab.it |
 |
|
|







