| Autore |
Discussione |
|
|
Lorenzaaaaa
Nuovo Arrivato

31 Messaggi |
 Inserito il - 09 dicembre 2010 : 15:59:40 Inserito il - 09 dicembre 2010 : 15:59:40




|
Qualcuno sa spiegarmi in dettaglio la formazione di una base di schiff? so che si forma tra un gruppo carbonile e un gruppo amminico ma non riesco a capire i vari passaggi...
grazie
|
|
|
|
|
chim2
Utente Attivo
  


2110 Messaggi |
 Inserito il - 09 dicembre 2010 : 16:23:22 Inserito il - 09 dicembre 2010 : 16:23:22




|
| � un'addizione nucleofila impossibile che non a trovi sul testo! |
 |
|
|
Caffey
Utente Attivo
  

Citt�: Perugia

1496 Messaggi |
 Inserito il - 09 dicembre 2010 : 16:37:59 Inserito il - 09 dicembre 2010 : 16:37:59




|
Ecco a te!
Formazione di un'aldimmina:
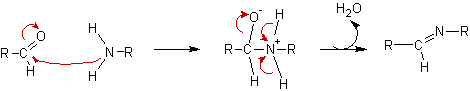
2,58 KB
 |
[...] Hunc igitur terrorem animi tenebrasque necessest
non radii solis neque lucida tela diei
discutiant, sed naturae species ratioque. [...]
Titus Lucretius Carus |
 |
|
|
chim2
Utente Attivo
  


2110 Messaggi |
 Inserito il - 09 dicembre 2010 : 16:39:10 Inserito il - 09 dicembre 2010 : 16:39:10




|
| http://it.wikipedia.org/wiki/Immine solo che il meccanismo presentato non ho idea di chi l'abbia scritto,cmq inizilamente c'� un caria + sull'N dopo che ha attaccato il C--O si libera un H+ poi successivamente questo forma H20+ che � un buon gruppo uscente su wiki � sbagliato perch� l'OH non esce neanche se lo si paga |
 |
|
|
chim2
Utente Attivo
  


2110 Messaggi |
 Inserito il - 09 dicembre 2010 : 16:48:57 Inserito il - 09 dicembre 2010 : 16:48:57




|
Citazione:
Messaggio inserito da Caffey
Ecco a te!
Formazione di un'aldimmina:

2,58�KB

no attento quelle 2 frecce sul semiamminale sono sbagliate,l'acqua esce con E1 a dare lo ione imminio che ha 2 forme di risonanza solo la perdita del protone da la base di shiff
P.S. � preferibile usare il catalizzare acido altrimenti l'addizione � troppo lenta ma bisogna prestare attenzione ancora venga protonata l'ammina perdendo il carattere nucleofilo,quindi si fa a un pH 4-5 solitamente,inoltre la rxn � un equilibrio quindi ci vogliono le doppie frecce  |
 |
|
|
Caffey
Utente Attivo
  

Citt�: Perugia

1496 Messaggi |
 Inserito il - 09 dicembre 2010 : 17:16:53 Inserito il - 09 dicembre 2010 : 17:16:53




|
Mhm... Sulle doppie frecce hai ragione. Non c'ho pensato.
Tutto il resto � troppo complesso per un banale studente di medicina come me, quindi chiedo perdono.
La reazione, tuttavia, l'ho copiata pari pari dalle diapositive del mio professore di chimica e noi l'abbiamo studiata cos�. Magari l'ha semplificata per farcela capire...
Dopotutto a noi serve solo per capire le transaminazioni in biochimica (che sono enzimatiche e quindi del catalizzatore non ce ne frega niente). Tutto il resto non ci serve, non lo facciamo e quindi � un buco nero per me! Non ho neanche ben capito la tua spiegazione.
Se vuoi prendi pure l'immagine e correggila, non ci sono problemi!
Io speravo di fare qualcosa di utile...
 |
[...] Hunc igitur terrorem animi tenebrasque necessest
non radii solis neque lucida tela diei
discutiant, sed naturae species ratioque. [...]
Titus Lucretius Carus |
 |
|
|
chim2
Utente Attivo
  


2110 Messaggi |
 Inserito il - 09 dicembre 2010 : 17:20:24 Inserito il - 09 dicembre 2010 : 17:20:24




|
lo so che fai medicina infatti cercavo di farti capire il meccanismo per cultura   |
 |
|
|
Lorenzaaaaa
Nuovo Arrivato

31 Messaggi |
 Inserito il - 10 dicembre 2010 : 08:41:47 Inserito il - 10 dicembre 2010 : 08:41:47




|
scusate... ma io non ho capito perch� va via l'acqua... che senso ha? |
 |
|
|
Patrizio
Moderatore
  

Citt�: Barcellona

1914 Messaggi |
 Inserito il - 10 dicembre 2010 : 11:49:12 Inserito il - 10 dicembre 2010 : 11:49:12





|
Ci provo io, con tutte le condizioni dette da chim2
l'intemedio carbocationico non l'ho messo ma si formerebbe al terzo step
Immagine:
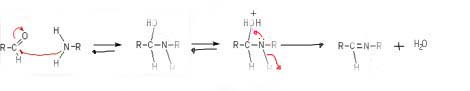
33,36 KB |

|
 |
|
|
nashita
Utente
 

Prov.: Puglia

1085 Messaggi |
 Inserito il - 10 dicembre 2010 : 11:51:29 Inserito il - 10 dicembre 2010 : 11:51:29




|
Patrizio non si forma l'intermedio carbocationico...
Nel terzo step , l'acqua viene eliminata per cui quella freccia cos� non l'ho capita,mentre il doppietto dell'azoto si ribalta portando alla formazione del doppio legame C-N . Poi la carica positiva non c'� nella terza struttura che hai scritto ma c'� nella quarta |
 |
 |
|
|
chim2
Utente Attivo
  


2110 Messaggi |
 Inserito il - 10 dicembre 2010 : 11:54:37 Inserito il - 10 dicembre 2010 : 11:54:37




|
Citazione:
Messaggio inserito da Patrizio
Ci provo io con tutte le condizioni dette da chim2
l'intemedio carbocationico non l'ho messo ma si formerebbe al terzo step
Immagine:
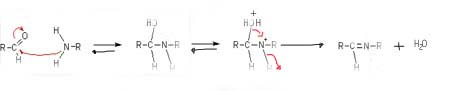
33,38�KB
ok va bene patrizio ma anche qui una precisazione sulle frecce:� il doppietto elettonico sull'N che espelle (facendo una 2 freccia) l'H2O quindi avremo uno ione con una carica + sull'N e poi espelle quel H+,
ok direi che � tutto:Lorenza ora puoi disegnarlo da sola!
P.S. l'H20 � un buon gruppo uscente a differenza di OH- che � una base forte e per farlo uscire ci vogliono condizioni d reazione pi� drastiche e temperature pi� alte.Poi ti consiglio ,Lorenza,come ti ho scritto sopra di aprire anche il libro perch� qui ci possiamo stare dietro anche 10 persone ma se non apri un testo di organica � difficile che comprendi tutto  |
 |
|
|
nashita
Utente
 

Prov.: Puglia

1085 Messaggi |
 Inserito il - 10 dicembre 2010 : 12:00:10 Inserito il - 10 dicembre 2010 : 12:00:10




|
Citazione:
Messaggio inserito da chim2
Citazione:
Messaggio inserito da Patrizio
Ci provo io con tutte le condizioni dette da chim2
l'intemedio carbocationico non l'ho messo ma si formerebbe al terzo step
Immagine:

33,38�KB
ok va bene patrizio ma anche qui una precisazione sulle frecce:� il doppietto elettonico sull'N che espelle (facendo una 2 freccia) l'H2O quindi avremo uno ione con una carica + sull'N e poi espelle quel H+,
ok direi che � tutto:Lorenza ora puoi disegnarlo da sola!
P.S. l'H20 � un buon gruppo uscente a differenza di OH- che � una base forte e per farlo uscire ci vogliono condizioni d reazione pi� drastiche e temperature pi� alte.Poi ti consiglio ,Lorenza,come ti ho scritto sopra di aprire anche il libro perch� qui ci possiamo stare dietro anche 10 persone ma se non apri un testo di organica � difficile che comprendi tutto 
chim, nell'immagine di patrizio cmq la carica positiva si forma dopo nella quarta struttura e non nella terza... |
 |
 |
|
|
nashita
Utente
 

Prov.: Puglia

1085 Messaggi |
 Inserito il - 10 dicembre 2010 : 12:04:03 Inserito il - 10 dicembre 2010 : 12:04:03




|
| Cmq ho visto che hai cambiato l'immagine, adesso � ok...manca solo la freccia di eliminazione dell'acqua :D e il protone si perde dopo la fomrazione dello ione imminio per ristabilire il catalizzatore acido |
 |
 |
|
|
Patrizio
Moderatore
  

Citt�: Barcellona

1914 Messaggi |
 Inserito il - 10 dicembre 2010 : 12:04:53 Inserito il - 10 dicembre 2010 : 12:04:53





|
| l'avevo corretto !! ...un attimo che arrivo ... devo gioire per i miei cloni positivi e fumarmi una sigaretta..torno subito |

|
 |
|
|
chim2
Utente Attivo
  


2110 Messaggi |
 Inserito il - 10 dicembre 2010 : 12:05:22 Inserito il - 10 dicembre 2010 : 12:05:22




|
| gli sar� sfuggito perch� la 2 � scritta bene, � proprio la chiusura del doppietto che chiude il legame quindi automaticamente si correggeva la carica + |
 |
|
|
nashita
Utente
 

Prov.: Puglia

1085 Messaggi |
 Inserito il - 10 dicembre 2010 : 12:06:17 Inserito il - 10 dicembre 2010 : 12:06:17




|
Citazione:
Messaggio inserito da Patrizio
l'avevo corretto !! ...un attimo che arrivo ... devo gioire per i miei cloni positivi e fumarmi una sigaretta..torno subito
sisi infatti io ti ho scritto prima che correggessi l'immagine, ho visto ora che hai cambiato :P |
 |
 |
|
|
Patrizio
Moderatore
  

Citt�: Barcellona

1914 Messaggi |
 Inserito il - 10 dicembre 2010 : 13:14:56 Inserito il - 10 dicembre 2010 : 13:14:56





|
| bhe' ..tutto � bene quel che finisce bene, con i vostri commenti e le immagini credo sia ok |

|
 |
|
|
nashita
Utente
 

Prov.: Puglia

1085 Messaggi |
 Inserito il - 10 dicembre 2010 : 15:34:02 Inserito il - 10 dicembre 2010 : 15:34:02




|
Citazione:
Messaggio inserito da Caffey
Tutto il resto � troppo complesso per un banale studente di medicina come me, quindi chiedo perdono.
La reazione, tuttavia, l'ho copiata pari pari dalle diapositive del mio professore di chimica e noi l'abbiamo studiata cos�. Magari l'ha semplificata per farcela capire...
Dopotutto a noi serve solo per capire le transaminazioni in biochimica (che sono enzimatiche e quindi del catalizzatore non ce ne frega niente). Tutto il resto non ci serve, non lo facciamo e quindi � un buco nero per me! Non ho neanche ben capito la tua spiegazione.
Se vuoi prendi pure l'immagine e correggila, non ci sono problemi!
Io speravo di fare qualcosa di utile...
Caffey, a me sembra che tu sappia anche di pi� di quello che appunto uno studente di medicina di solito deve sapere riguardo l'organica, lo dico anche in riferimento ad altri tuoi post di organica presenti nel forum di biochimica 
comunque volevo solo puntualizzare che in biochimica i meccanismi catalitici enzimatici avvengono o con catalisi acido base,con catalisi metalliche con catalisi covalent. Per cui il ruolo di catalizzatori acido/base � dato dalle stesse catene laterali degli AA che si comportano da Acido e da base nel sito attivo dell'enzima. (Per esempio se consideri il meccanismo della chimotripsina, la fase di acilazione promossa dalla serina 195 pu� avvenire proprio grazie alle propriet� acido base dell'Hys 57 e Asp102). |
 |
 |
|
|
Caffey
Utente Attivo
  

Citt�: Perugia

1496 Messaggi |
 Inserito il - 10 dicembre 2010 : 16:10:13 Inserito il - 10 dicembre 2010 : 16:10:13




|
Grazie nashita! Sei molto gentile!
Certo che la catalizzazione avviene grazie a quei meccanismi, lo so. Soltanto che a noi non interessano pi� di tanto se non cos� in generale, come potrai capire, quindi neanche a chimica generale ci concentriamo troppo sulla catalisi. A noi basta sapere quale enzima � coinvolto in una reazione e in alcuni sporadici casi qual � il meccanismo (tipo le transaminazioni e deaminazioni PLP-dipendenti). In fin dei conti la biochimica a noi serve solo per capire la fisiologia, la patogenesi e per intuire le conseguenze fenotipiche date da mutazioni a carico degli enzimi e dei trasportatori.
 |
[...] Hunc igitur terrorem animi tenebrasque necessest
non radii solis neque lucida tela diei
discutiant, sed naturae species ratioque. [...]
Titus Lucretius Carus |
 |
|
| |
Discussione |
|










