| |||
| Forum |
| Registrati Discussioni Recenti Preferiti Utenti Cerca Regolamento RSS Statistiche |
|
I libri
consigliati:  Metodologie di base per la biochimica e la biotecnologia David Ballou, Alexander Ninfa  DNA ricombinante Michael Gilman, James D. Watson, Jan Witkowski, Ma  Flussi e riflussi. Indagine sull'origine di una teoria scientifica Lucio Russo Altri Libri |
|
|
Risorse di Biochimica:
|
Quanto � utile/interessante questa discussione:
|
|||||||||||||||||||||||
Quanto � utile/interessante questa discussione:
|
|

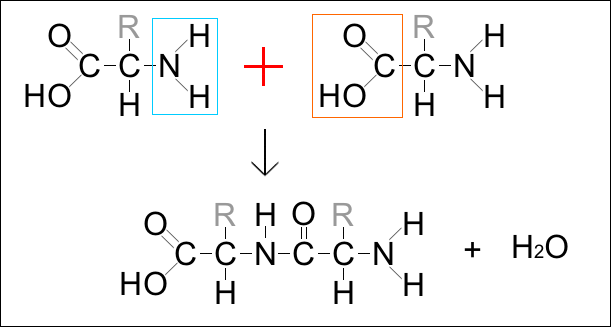
 il meccanismo di reazione che porta alla formazione di un legame peptidico in generale � una sostituzione nucleofila acilica?vorrei sapere se � cos� dato che l' ammide � un derivato dell' acido carbossilico e tutti i derivati degli acidi carbossilici per quanto ne sappia si formano in tal modo!!Poi ho letto che nelle cellule il meccanismo di formazione del legame peptidico � diverso e richiede l' attivazione del carbossilico da parte del trn.Ora la mia seconda domanda a tal proprosito �:� richiesta l' attivazione da parte del trn perch� il gruppo OH del carbossilico � un nucleofilo pi� forte rispetto all' NH2 del secondo amminoacido che attacca il primo amminoacido?quindi OH del carbossilico avrebbe difficolt� a staccarsi dal gruppo carbossilico perci� non avviene una normale sostituzione acilica?? vorrei avere dei chiarimenti!!grazie
il meccanismo di reazione che porta alla formazione di un legame peptidico in generale � una sostituzione nucleofila acilica?vorrei sapere se � cos� dato che l' ammide � un derivato dell' acido carbossilico e tutti i derivati degli acidi carbossilici per quanto ne sappia si formano in tal modo!!Poi ho letto che nelle cellule il meccanismo di formazione del legame peptidico � diverso e richiede l' attivazione del carbossilico da parte del trn.Ora la mia seconda domanda a tal proprosito �:� richiesta l' attivazione da parte del trn perch� il gruppo OH del carbossilico � un nucleofilo pi� forte rispetto all' NH2 del secondo amminoacido che attacca il primo amminoacido?quindi OH del carbossilico avrebbe difficolt� a staccarsi dal gruppo carbossilico perci� non avviene una normale sostituzione acilica?? vorrei avere dei chiarimenti!!grazie