Una giornata in laboratorio: ecco come si estrae il DNA!
Benvenuti in questo secondo giro in laboratorio!
L’ultima volta abbiamo estratto proteine da un campione biologico, e le abbiamo utilizzate in qualche esperimento. Come probabilmente saprete, le proteine sono sintetizzate dai ribosomi che incastrano assieme amminoacidi l’uno dopo l’altro in lunghe (o corte :P) catene seguendo il progetto scritto sull’RNA messaggero; a sua volta quest’ultimo viene ricopiato dal progetto originale che risiede nel nucleo della cellula, nel DNA.
Dato che noi biologi molecolari non ci facciamo mai gli affari nostri, oggi estraiamo DNA e andiamo a vedere che cos’ha da raccontarci.
Quest’oggi ci renderemo conto di come molte attività di laboratorio, pur concentrandosi su aspetti diversi, convergano a livello metodologico. Mi spiego meglio: per estrarre DNA da qualcosa, lo si prende, lo si frulla in qualche maniera, si fa in modo che quello che vogliamo estrarre sia solubile in qualcosa che aggiungiamo al campione (e possibilmente si fa pure in modo che quello che non vogliamo estrarre non sia solubile nel medesimo liquido) e si procede con barbatrucchi fisico/chimici levando dalla soluzione tutto quello che non ci interessa. In principio è quello che abbiamo fatto l’altra volta; vediamo oggi come facciamo a procurarci del viscido, traslucido e moccioso DNA (oppure del duro, bianco e cristallino DNA – dipende da come e dove lo volete ^_^).
Sminuzzare il tessuto (come in questa figura dell’articolo precedente) è un buon punto di partenza, ma non basta.
Dopo il giro col frullatore, lascio in incubazione nel bagnetto termostatato (che vedete nella foto) per tutta la notte i campioni da cui voglio estrarre il DNA in compagnia di un enzima (una proteina) che si chiama Proteinasi K. Le provettine galleggiano nel liquido riscaldato nei galleggini che vedete, e a 50 °C questo enzima digerisce tutte le proteine che incontra (inclusa sé stessa). Questa digestione enzimatica serve a disgregare il tessuto e a liberare il DNA dagli istoni su cui si avvolge, permettendoci di ottenere DNA più pulito (da residui di proteine).
Dopo una breve centrifugata (come è fatta una centrifuga? qui), tutta la robaccia indigerita si deposita sul fondo della provetta. Che cosa rimane in soluzione? Con ogni probabilità l’RNA ce lo siamo giocato durante la notte a 50 °C (1), quindi mi aspetto pezzi di proteine, zuccheri, amminoacidi liberi, grassi, nucleotidi liberi, ioni di sali vari e – naturalmente – filamenti di DNA paciosamente in soluzione acquosa. E’ ora di iniziare a separare tutte queste cose!
Alla soluzione acquosa con dentro tutta quella roba là ho aggiunto fenolo e cloroformio. Il fenolo è un alcool interessante: è un solido (ah, quando ne ho ordinato un Kg per sbaglio anzichè la soluzione di un litro!) che però con buona buona volontà può essere sciolto in acqua (grazie, gruppo OH!). Di acqua però non gliene piace troppa, prende solo qualche molecola per essere solubilizzato e quella in eccesso la scarta (l’acqua in eccesso forma una fase sopra quella del fenolo); per questo nei protocolli si parla di fenolo saturo. E’ un denaturante di proteine ed è lipofilo, e assieme al cloroformio serve a sciogliere tutto quanto è solubile in un solvente organico (residui di proteine, lipidi). Infatti, dopo una breve centrifugata…
…il campione si separa in due fasi chiaramente riconoscibili. Sotto (2) abbiamo la fase organica: fenolo, cloroformio, grassi, proteine, robaccia varia. Abbiamo poi un’interfaccia, che contiene solitamente dei detriti grossi e indigeriti che erano rimasti in soluzione; al di sopra, la fase acquosa ripulita da molte schifezze e contenente il DNA. Quello che vogliamo fare è togliere il DNA da là per scioglierlo in acqua (3) e non in un liquido con dentro tutti i sali e i residui tissutali del mondo, dove si trova adesso.
Ma come facciamo? Semplice! Rendiamo insolubile il DNA. Ora, il DNA è solubile in acqua, ma non è solubile in etanolo. L’etanolo però è completamente solubile in acqua: il trucco è aggiungere abbastanza etanolo all’acqua da rendere insolubile il DNA. Guardate come in questo video!
Dopo una breve centrifugata di un minuto, il DNA si pelletta contro la parete della provetta.
Nella provetta potete osservare delle gocce di liquido (una soluzione di acqua ed etanolo) e nella parte più bassa della provetta (in alto nella figura) un pallozzo bianco: il DNA che poco fa era sospeso come filamenti insolubili nel video.
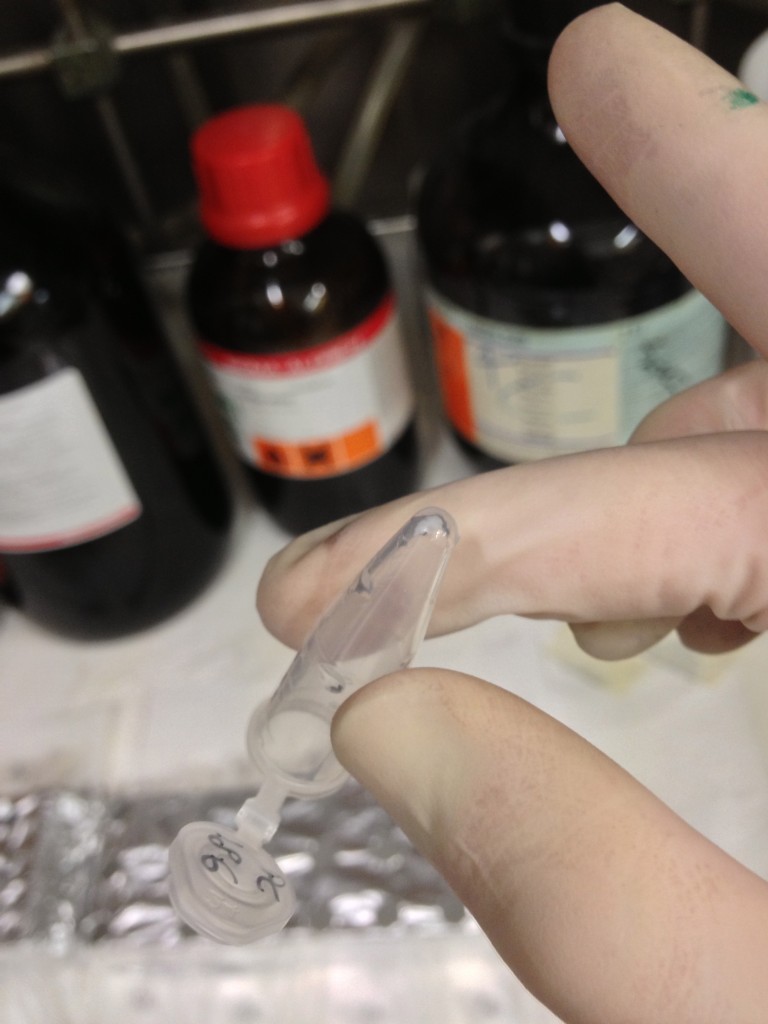
Lasciamo asciugare una decina di minuti sotto cappa chimica, e siamo pronti a risospendere il DNA in acqua! Il trucco è non seccare troppo la “pallina bianca”: l’etanolo evapora molto in fretta: più in fretta dell’acqua che è ancora presente. Il DNA comincia a reidratarsi assumendo l’aspetto di una pallina traslucida e semitrasparente dall’aspetto gommoso: è questo il momento adatto per risospenderlo in acqua! Se aspettiamo, anche quest’acqua evaporerà e il DNA salificherà col sodio (probabilmente) presente nella soluzione, e sarà molto più duro da solubilizzare ancora in acqua.
A questo punto, se non ho fretta aggiungo 100 microlitri di acqua e metto tutto in frigo per tutta notte (noi che ce la tiriamo diciamo overnight): il giorno dopo sarà tutto bello rispospeso e pronto per essere utilizzato!
Utilizzato per cosa? Questa domanda ha tante (ma davvero tante) risposte, ne vedremo insieme qualcuna nelle prossime puntate!
Piermatteo
Note
(1) le RNAsi sono gli enzimi che distruggono, o meglio digeriscono l’RNA. Sono fra gli enzimi più resistenti in assoluto, in grado di resistere anche alla bollitura. Prima di essere distrutte dalla Proteinasi K, le RNAsi presenti nel tessuto hanno tutto il tempo di sfasciare l’RNA presente. In più, nonostante sia chimicamente molto simile, l’RNA è meno stabile in acqua e si idrolizza (rompe) spontaneamente. Dopo tutto, non ha – come il DNA – il compito di memorizzare per lungo tempo un’informazione.
(2) Una leggenda vuole che una volta ogni tanto avvenga una famigerata inversione di fase, in cui sopra ci sia la fase organica e sotto la fase acquosa. Per questo, è sempre meglio tenere fino alla fine dell’estrazione tutte le provette senza buttarle, per poter eventualmente recuperare la vera fase acquosa. In tutta la vita non ho mai osservato questo fenomeno, ma conservare le provette fino alla fine è sempre una buona idea, se rovesciate qualcosa, un po’ di DNA lo recuperate dal pochettino di fase acquosa che lasciate vicino all’interfaccia.
NOTA AGGIUNTIVA: Molti usano del TE (Tris – EDTA) per mantenere il DNA in soluzione, perchè il pH del TE aiuta a sciogliere il DNA e la bassa concentrazione di EDTA inibisce il funzionamento di eventuali DNAsi, ma io ho sempre utilizzato l’acqua per preparazioni iniettabili della farmacia. Per tre ragioni: è assolutamente pura e di ottima qualità, il DNA è praticamente invulnerabile (se non gli fate capitare qualcosa apposta) e la faccia del farmacista durante questo dialogo:
Piermatteo: avete fialette da 5 ml di acqua per preparazioni iniettabili?
Farmacista: sì, quante gliene servono?
Piermatteo: voi quante ne avete?
è assolutamente impagabile e non ci rinuncerei mai!
Tag:centrifuga, DNA, estrazione DNA, inversione di fase, istoni, pellet, proteinasi K
seguici anche su Facebook!








Complimenti e grazie per queste lezioni di laboratorio. Non se ne trovano molte in giro.
Grazie mille davvero.
Continuerò a seguirvi.